ενότητα:Στοιχεία της
ατμόσφαιρας
Η μεταβολή φάσεως του νερού καταλήγει σε
μεταβολή θερμότητος στην ατμόσφαιρα. Η
απαιτούμενη θερμότητα για να μετατρεπτεί 1 gm
νερού σε υδρατμό υπό σταθερή πίεση λέγεται λανθάνουσα
θερμότητα εξαερώσεως ![]() και είναι η μεταβολή
της ολικής ενθαλπίας του συστήματος
νερού-υδρατμού. Η ολική ενέργεια που έχει ένα
σύστημα είναι η ενθαλπία h η οποία δίνεται από:
και είναι η μεταβολή
της ολικής ενθαλπίας του συστήματος
νερού-υδρατμού. Η ολική ενέργεια που έχει ένα
σύστημα είναι η ενθαλπία h η οποία δίνεται από:
![]()
διαφορίζοντας:
![]()
και υπό σταθερή πίεση απλοποιείται σε:
![]()
Η λανθάνουσα θερμότητα από μια φάση σε άλλη δίνεται από:
![]()
και έτσι έχομε:
![]()
αλλά ![]()
![]()
![]() και έτσι:
και έτσι:
![]()
αντικαθιστώντας ![]() με R/Τ. Διαφορίζοντας με την
θερμοκρασία Τ έχομε:
με R/Τ. Διαφορίζοντας με την
θερμοκρασία Τ έχομε:
![]()
και καταλήγομε στο νόμο του Kirchoff:
![]()
Ομοίως έχομε για την αλλαγή φάσεως από πάγο σε υδρατμό την λανθάνουσα θερμότητα εξαχνώσεως:
![]()
και για την αλαγή φάσεως από πάγο σε νερό την λανθάνουσα θερμότητα τήξεως:
![]()
Οι θερμότητες σε cal/gm (όπου 4,184 J = 1 cal) έχουν τις εξής τιμές:
= 0,503 + 1,767
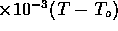
![]() = 1,007
= 1,007
![]() = 0,447
= 0,447
Βλέπομε ότι για τον υδρατμό ![]()
![]() όπου
όπου ![]() =0,112 cal/gm.
Ολοκληρώνοντας έχομε για Τ
=0,112 cal/gm.
Ολοκληρώνοντας έχομε για Τ ![]()
![]() και
και ![]() =597,3 cal/gm όταν Τ=
=597,3 cal/gm όταν Τ= ![]() :
:
![]()
ενώ για Τ ![]()
![]() έχομε:
έχομε:
![]()
και
![]()
όπου ![]() =667,0
cal/gm και
=667,0
cal/gm και ![]() =79,7
cal/gm όταν Τ=
=79,7
cal/gm όταν Τ= ![]() :
:
ενότητα:Στοιχεία της ατμόσφαιρας